W Unii Europejskiej mamy zarejestrowane i dopuszczone do sprzedaży 4 leki przyczynowe, leki nowej generacji stosowane u części pacjentów z mukowiscydozą (żaden nie jest refundowany w Polsce). Lekami przyczynowymi w mukowiscydozie nazywamy preparaty lecznicze, których substancje czynne wpływają na przyczynę tej choroby, a nie objawy. Przyczyną mukowiscydozy jest nieprawidłowe działanie kanałów chlorkowych w wyniku problemów z formowaniem i działaniem białek CFTR. Wszystko z powodu mutacji CFTR.
Klasy mutacji genu CFTR w mukowiscydozie
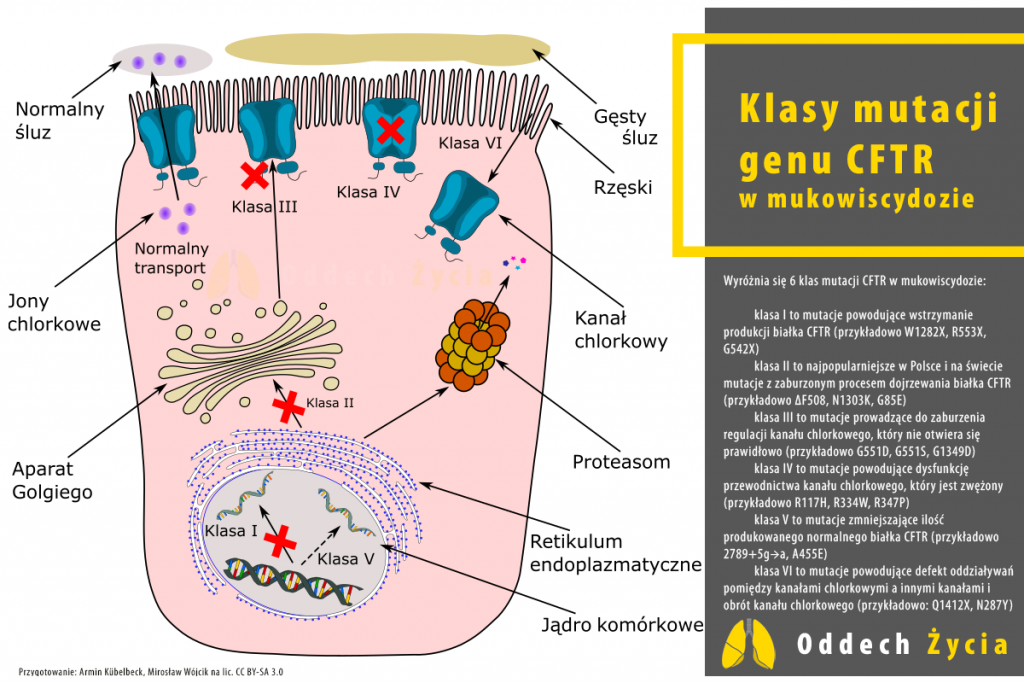
Próbując wyjaśnić czym są i jak działają modulatory CFTR obecne w lekach przyczynowych stosowanych u pacjentów z mukowiscydozą trzeba mieć na względzie dużą różnorodność mutacji CFTR. Pacjent z mukowiscydozą posiada dwie mutacje CFTR, po jednej od każdego rodzica. Obecnie znamy ponad 2 tysiące różnych mutacji CFTR należących do sześciu klas:
- klasa I to mutacje powodujące wstrzymanie produkcji białka CFTR (przykładowo W1282X, R553X, G542X).
- klasa II to najpopularniejsze w Polsce i na świecie mutacje z zaburzonym procesem dojrzewania białka CFTR (przykładowo ΔF508, N1303K, G85E)
- klasa III to mutacje prowadzące do zaburzenia regulacji kanału chlorkowego, który nie otwiera się prawidłowo (przykładowo G551D, G551S, G1349D)
- klasa IV to mutacje powodujące dysfunkcję przewodnictwa kanału chlorkowego, który jest zwężony (przykładowo R117H, R334W, R347P)
- klasa V to mutacje zmniejszające ilość produkowanego normalnego białka CFTR (przykładowo 2789+5g→a, A455E)
- klasa VI to mutacje powodujące defekt oddziaływań pomiędzy kanałami chlorkowymi a innymi kanałami i obrót kanału chlorkowego (przykładowo: Q1412X, N287Y).
Mutacje klasy I-III zalicza się do grupy mutacji najcięższych, mutacje klasy IV-VI do grupy mutacji łagodnych*.
Rodzaje modulatorów CFTR
Istnieją trzy główne typy modulatorów CFTR:
- potencjatory CFTR,
- korektory CFTR,
- wzmacniacze CFTR.
Potencjatory CFTR
Prawidłowo zbudowane i działające białko CFTR przypomina kształtem tunel i w zależności od tego czy jest otwarte, czy zamknięte steruje przepływem jonów chlorkowych. Potencjatory CFTR zwiększają aktywność białka CFTR, utrzymując tunel otwarty dla jonów.
Potencjatory działają tylko w przypadku, gdy białko CFTR dotarło do powierzchni komórki, dlatego mają zastosowanie u pacjentów z mutacjami klasy III i IV, zwiększając wydajność pracy niewystarczającej ilości prawidłowych białek CFTR albo poprawiając wydajność działania białek CFTR z zaburzoną regulacją. Mogą być też stosowane w połączeniu z korektorami i wzmacniaczami u pacjentów z innymi klasami mutacji CFTR.
Do grupy potencjatorów CFTR zarejestrowanych w USA, UE, Australii i Kanadzie oraz innych krajach należy iwakaftor (łac. ivacaftorum, ang. ivacaftor). Iwakaftor to wielofunkcyjny organiczny związek chemiczny z grupy chinolonów, który zwiększa otwarcie kanału chlorkowego tworzonego przez białko CFTR poprzez fosforylację, u pacjentów z mutacjami: E56K, G178R, S549R, K1060T, G1244E, P67L, E193K, G551D, A1067T, S1251N, R74W, L206W, G551S, G1069R, S1255P, D110E, R347H, D579G, R1070Q, D1270N, D110H, R352Q, S945L, R1070W, G1349D, R117C, A455E, S977F, F1074L, R117H, S549N, F1052V, D1152H oraz potencjalnie także w: 3849+10kbC->T, 2789+5G->A, 3272-26A->G, 711+3A->G, E831X.
Do grupy potencjatorów należą również substancje w fazie badań laboratoryjnych i klinicznych niedostępne na razie dla pacjentów np.:
- GLPG2451 i GLPG1837 opracowywane przez Galapagos we współpracy z Abbvie;
- FDL176 opracowywany przez Flatley Discovery Lab;
- QBW251 opracowywany przez Novartis;
- PTI-808 opracowywany przez Proteostasis Therapeutics.
Trwają również badania znanych od dawna substancji leczniczych, które mogłyby mieć potencjalnie zastosowanie jako potencjatory CFTR. Mowa tutaj m.in. o znanej kwercetynie i genisteinie. Kwercytyna występuje naturalnie w kwiatach głogu i kasztanowca, ale też wielu innych roślinach. Genisteina występuje w roślinach bobowatych i strączkowych, a jej najbogatszym źródłem jest soja. Niestety uzyskanie w organizmie stężenia substancji potrzebnego do jej efektywnego działania z naturalnych źródeł (diety, suplementacji) jest bardzo trudne do osiągnięcia w przypadku i kwercetyny i genisteiny.
Korektory CFTR
Białko CFTR aby było w pełni funkcjonalne musi przyjąć odpowiedni kształt. Część mutacji CFTR, z klasy II, powoduje zaburzenie procesu dojrzewania białka CFTR, co w konsekwencji prowadzi do nieprawidłowego kształtu – budowy przestrzennej 3D. Korektory CFTR ułatwiają formowanie prawidłowej struktury przestrzennej białka CFTR, ale nie wpływają na wydajność pracy kanału chlorkowego, dlatego obecnie zarejestrowane i dopuszczone do sprzedaży leki przyczynowe zawierają w swoim składzie dodatkowo potencjator w postaci iwakaftoru.
Do grupy korektorów CFTR należą lumakaftor, tezakaftor i eleksakaftor, z czego dwa pierwsze zarejstrowane są i dopuszczone od sprzedaży w preparatach dostępnych na całym świecie, w tym Unii Europejskiej, a ostatni, eleksakaftor dostępny jest na ten moment w leku zarejestrowanym tylko w USA (oczekuje rejestracji w Unii Europejskiej).
PTI-801 jest opracowanym przez Proteostasis Therapeutics korektorem CFTR.
Wzmacniacze CFTR
Niektóre mutacje CFTR zakłócają mechanizm prawidłowego odczytu kodu genetycznego w procesie tworzenia białek CFTR, w wyniku czego powstaje bardzo mała ilość białka CFTR. Wzmacniacze CFTR zwiększają produkcję białka CFTR.
PTI-428 jest opracowanym przez Proteostasis Therapeutics wzmacniaczem CFTR.
* – “Classification of CFTR mutation classes”, The Lancet S2213-2600(16)30188-6 (2016), “Mukowiscydoza choroba wielonarządowa” pod redakcją prof. Doroty Sands (2018). “Genetyczne podłoże mukowiscydozy”; “CFTR genotype and clinical outcomes of adult patients carried as cystic fibrosis disease” Bonadia LC, de Lima Marson FA, Ribeiro JD, Paschoal IA, Pereira MC, Ribeiro AF, Bertuzzo C.